Klinische Studie der Phase I zur intrakraniellen Injektion von CAR-modifzierten NK-Zellen in Patienten mit rezidiviertem, HER2-positivem Glioblastom
Mitantragsteller:
Prof. Dr. med. Torsten Tonn: DRK-Blutspendedienst
PD Dr. med. Michael Burger, Prof. Dr. med. Joachim Steinbach, Prof. Dr. med. Christian Senft: Zentrum der Neurologie und Neurochirurgie, Universitätsklinikum Frankfurt
Prof. Dr. med. Karl Plate: Edinger Institut, Universitätsklinikum Frankfurt
Projektpartner:
Universitätsklinikum Frankfurt
DRK-Blutspendedienst Frankfurt und Dresden
Projektvorstellung:
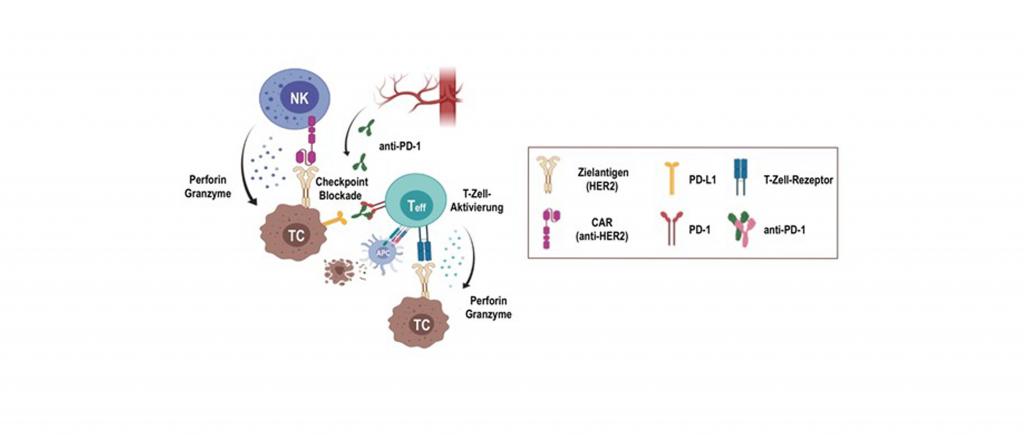
Die Expression von chimären Antigenrezeptoren (CARs) in zytotoxischen Lymphozyten ist eine vielversprechende Strategie für die adoptive Krebsimmuntherapie mit Effektorzellen definierter Spezifität. CARs sind Transmembranproteine, die aus einem extrazellulären, tumorspezifischen Antikörperfragment (scFv) bestehen, das mit einer oder mehreren intrazellulären Signaldomänen verknüpft ist, die nach Erkennung des Zielantigens die Aktivierung der Effektorzelle auslösen. Neben T-Lymphozyten stellen auch natürliche Killerzellen (NK-Zellen) eine wertvolle Effektorzellpopulation für solche Ansätze dar. Basierend auf der klinisch einsetzbaren humanen NK-Zelllinie NK-92 wurde der kontinuierlich expandierende Zellklon NK-92/5.28.z abgeleitet, der einen CAR mit Spezifität für das Tumor-assoziierte Antigen HER2 (ErbB2) enthält, das bei einem hohen Anteil an Glioblastomen und vielen anderen soliden Tumoren überexprimiert vorliegt.
GMP-konforme Verfahren zur Herstellung von klinischen Dosen von NK-92/5.28.z-Zellen wurden entwickelt und die Investigator-initiierte klinische Phase-I-Studie CAR2BRAIN (NCT03383978, clinicaltrials.gov) wurde begonnen. Zunächst wurde diese Studie als monozentrische Studie am Zentrum für Neurologie und Neurochirurgie des Universitätsklinikums Frankfurt bei Patienten mit rezidiviertem, HER2-positivem Glioblastom durchgeführt. Im kürzlich abgeschlossenen ersten Teil der Studie zur Dosiseskalation wurden die Patienten während einer Rezidivoperation durch direkte Injektion einer Einzeldosis von NK-92/5.28.z-Zellen in die Wand der Resektionshöhle behandelt, um die Durchführbarkeit und Sicherheit dieses Ansatzes zu prüfen.
Im zweiten Teil der nun von der Else Kröner-Fresenius-Stiftung geförderten Studie erhalten Patienten der Expansionskohorte zusätzlich zu der ersten intraoperativen Injektion von NK-92/5.28.z-Zellen weitere Injektionen der Zellen in die Resektionshöhle durch einen implantierten Katheter und ein Reservoir. Mehrere weitere Studienzentren in Deutschland werden zu diesem Teil des Protokolls als multizentrische Studie beitragen. Ausgehend von vielversprechenden Daten in präklinischen Glioblastom-Modellen wurde das Protokoll um eine zusätzliche Kohorte von Patienten erweitert, die mit einer Kombination aus NK-92/5.28.z-Zellen und einem anti-PD-1 Immun-Checkpoint-Inhibitor behandelt werden (CAR2BRAIN-CHECK).
Weiterführende Informationen:
https://georg-speyer-haus.de/staff/wels-forschung/
https://www.uct-frankfurt.de/fuer-aerzte/klinische-studien/studienregister.html
https://clinicaltrials.gov/show/NCT03383978